Микробная память. Новое открытие объясняет, почему не работают антибиотики
МОСКВА, 29 ноя — РИА Новости, Владислав Стрекопытов. Некоторые микроорганизмы обладают не только коллективным разумом, но и памятью, причем порой "воспоминания" передают по наследству. К такому сенсационному выводу пришли американские ученые. Открытие может стать отправной точкой в разработке новых стратегий борьбы с бактериальной устойчивостью к антибиотикам.
Коллективный интеллект
В середине 1960-х биологи заметили, что при определенных обстоятельствах — стрессе или изменении условий среды — бактерии демонстрируют способность к самоорганизации, а их сообщества ведут себя как единое целое.
Так родилась концепция коллективного микробного интеллекта, основанная на предположении о том, что бактериальные колонии по своей организации подобны нейронным сетям. Микроорганизмы, получившие входные данные в виде химических сигналов, обрабатывают их и передают другим членам колонии.
Создателем научного направления, изучающего коммуникационные связи между микроорганизмами, — социомикробиологии — стал американский биолог Эверетт Питер Гринберг. В 1994-м он доказал, что экспрессия генов, а следовательно и поведение бактерий, меняется в зависимости от количества клеток. Этот механизм взаимодействия ученый назвал чувством кворума.
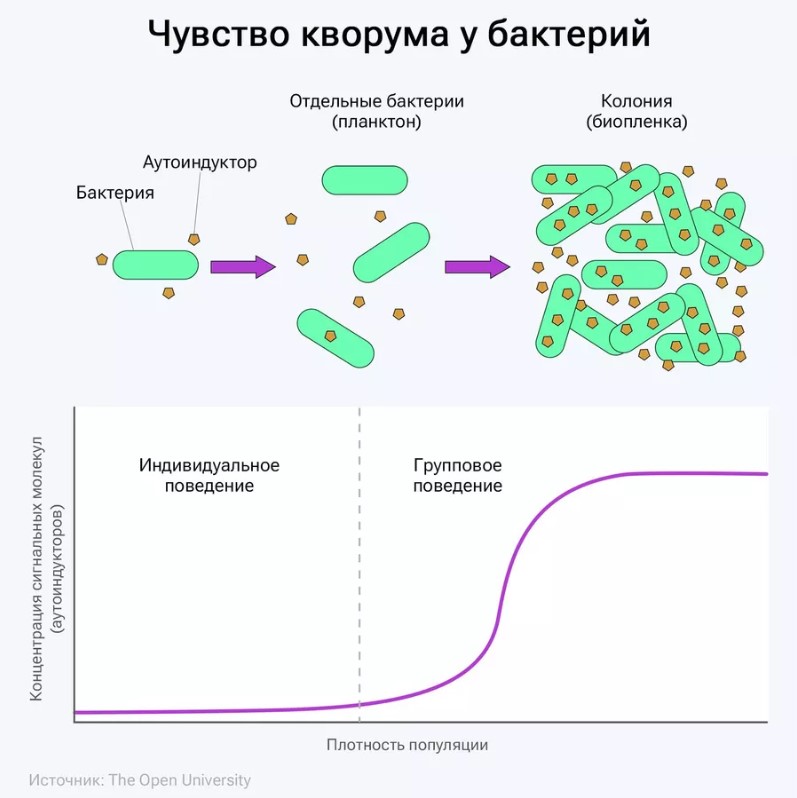
При определенных условиях бактерии выделяют в окружающую среду пептиды, известные как аутоиндукторы. Если плотность бактериальной популяции увеличивается, их концентрация тоже растет. Когда она достигает определенного уровня, аутоиндуктор может запустить транскрипцию специфических генов во всех клетках бактериальной колонии. Резкий выброс аутоиндукторов и возникающий при этом механизм обратной связи фиксируют переход от самостоятельного (планктонного) существования микроорганизмов к групповому поведению.
© Иллюстрация РИА Новости
По мере увеличения плотности популяции бактерий в определенный момент резко возрастает высвобождение сигнальных молекул (аутоиндукторов) во внеклеточную среду, что сопровождается изменением поведения с индивидуального (планктонного) на групповое
От биопленок к клеточной памяти
Дальнейшие исследования привели Гринберга и его коллег к открытию биопленок, возникающих в результате объединения тысяч и миллионов бактериальных клеток. Биопленки могут формироваться как на неорганических поверхностях, так и на живых тканях — зубах, внутренних стенках кишечника, а также в дыхательных путях и легких.
Пленочные колонии имеют массу биологических преимуществ по сравнению с отдельными микроорганизмами. При площадном расположении увеличивается доступ к питательным веществам, заметно возрастает устойчивость, в том числе — к воздействию антибиотиков. Кроме того, бактерии, объединяясь в пленки, меняют свои поверхностные антигены, и их перестает распознавать иммунная система.
Примечательно, что в образовании пленочных колоний могут совместно участвовать бактерии разных видов. Трудноизлечимые бактериальные инфекции — кишечные, легочные, урогенитальные, гинекологические — нередко связаны с образованием таких мультипатогенных биопленок.
В 2020-м ученые из Калифорнийского университета в Сан-Диего под руководством профессора кафедры молекулярной биологии Гюроля Зюэля описали новую форму коммуникации внутри биопленок. Наблюдая за колониями сенной палочки Bacillus subtilis, они обнаружили, что бактерии обмениваются информацией и координируют свои действия не только химическим путем, но и с помощью электрических сигналов, проходящих по ионным каналам.
Оказалось, что передача этих сигналов меняет свойства клеточных мембран и бактерии таким образом могут хранить информацию о прошлых состояниях. Ученые предположили, что подобные изменения служат своеобразной формой коллективной бактериальной памяти. Дело в том, что примерно так же реагируют на электрические сигналы клетки мозга — нейроны.
Память поколений
Бактериальную память, основанную на мембранном потенциале, можно назвать рабочей, или оперативной. Изменения в белках мембраны сохраняются несколько часов после первичного электрического или светового импульса, а затем исчезают. Но недавно биологи из Техасского университета в Остине и Университета Делавэра обнаружили, что бактерии, организованные в биопленки, способны хранить информацию в течение длительного времени и даже передавать ее из поколения в поколение.
Объектом исследования стали колонии кишечной палочки Escherichia coli. Эти бактерии — одна из самых хорошо изученных форм жизни на Земле. Ученые обнаружили у них аналог системы памяти, которая позволяет сохранять всю жизнь и передавать по наследству определенную информацию об окружающей среде.
На первой стадии эксперимента авторы подвергли клетки Escherichia coli воздействию различных факторов, чтобы увидеть, при каких условиях они лучше самоорганизуются. Выяснилось, что важнейшее условие формирования биопленок — уровень железа внутри клеток. При его недостатке бактерии собираются в так называемые рои и с помощью жгутиков устремляются в направлении роста концентраций этого элемента.
Меняя содержание железа в среде, биологи научились управлять "роением" бактерий. При этом заметили, что более "опытные" микроорганизмы, уже испытавшие дефицит клеточного железа, в следующий раз быстрее других объединялись и двигались в сторону его источника.
Продолжив наблюдения, ученые выяснили, что "воспоминания" о том, как надо себя вести в кризисной ситуации, сохранялись и у потомков "опытных" бактерий как минимум на протяжении четырех поколений, а к седьмому исчезали безвозвратно. Это первый официально подтвержденный факт наличия наследственной памяти у микроорганизмов.

© The University of Texas at Austin
Бактериальный рой Escherichia coli в лабораторной чашке
В поисках бактериального кода
Биологи считают бактериальную память важнейшим механизмом, обеспечивающим адаптацию и эволюцию микробов в изменяющихся условиях окружающей среды. В частности, эта память играет важнейшую роль в развитии резистентности (устойчивости) к антибиотикам, которая стала одной из самых актуальных проблем современной медицины.
Исследователи отмечают, что устойчивые к антибиотикам бактериальные клетки, как правило, имеют сбалансированный уровень железа. То есть они максимально стабильны и легко образуют пленочные покрытия. Есть вероятность, что, управляя уровнем железа, можно воздействовать на патогены, снижая их резистентность.
На следующем этапе исследований калифорнийские ученые планируют до конца разобраться в молекулярных механизмах формирования бактериальной памяти.
"У бактерий нет нейронов, синапсов и нервной системы, но они могут собирать информацию из окружающей среды, хранить эти данные и быстро получать к ним доступ позже в своих интересах, — приводятся в пресс-релизе слова первого автора статьи Сувик Бхаттачарья, научного сотрудника кафедры молекулярной биологии Техасского университета. — В конечном счете чем больше мы знаем о поведении бактерий, тем легче с ними бороться. Уровень железа, от которого зависит вирулентность патогенов, может стать мишенью для терапии".
Авторы предполагают, что механизм накопления и хранения информации в бактериальных клетках чем-то похож на принцип работы компьютерной памяти. А кодом, программирующим сложное поведение микробов, в данном случае становится уровень железа. Но таких кодирующих факторов может быть еще много. Ученые не исключают, что появится биокомпьютер, в котором информация будет передаваться с помощью электрических сигналов, а записываться — на клеточных оболочках бактерий.
